
– Den nye nasjonale handlingsplanen for kliniske studier ble publisert 11. januar i år. Det er den første i sitt slag, og den dekker hele helsetjenesten. Handlingsplanen er et resultat av mange gode møter og mange gode innspill fra mange aktører, sier seniorrådgiver i Helse- og omsorgsdepartementet, Marianne van der Wel.
Stor interesse
Helse- og omsorgsdepartementet hadde håpet på en stor, fysisk lansering av planen som så mange har ventet spent på, men på grunn av pandemien endte de med en veldig stille en. Så stille at LMI, med Hege Edvardsen i spissen, tok grep. Departementet ble invitert til å – via streaming – fortelle mer om planen, og motta både skryt og forslag til forbedringer fra noen av de som har gitt innspill og ventet spent på resultatet: industrien, klinikerne, sykehusledere og pasienter. Det var stor interesse for møtet, med over 450 påmeldte, og departementet takket LMI, NorCrin, Inven2, Melanor og Innovasjon Norge for initiativet til å arrangere webinaret.
Marianne van der Wel fortalte at handlingsplanen har to overordnede mål:
- at andelen pasienter i spesialisthelsetjenesten som deltar i kliniske studier er 5 prosent i 2025, og
- at antall kliniske studier er doblet i perioden 2021-2025
Disse målene skal nås gjennom ni innsatsområder:
1. Gi pasienter økte muligheter for å delta i kliniske studier
2. Bidra til at kliniske studier blir en mer integrert del av pasientbehandlingen
3. Bidra til økt samarbeid mellom tjenesten og næringslivet om kliniske studier
4. Bidra til raskere gjennomføring av kliniske studier
5. Bidra til flere studier i de kommunale helse- og omsorgstjenestene og tannhelsetjenesten
6. Øke kunnskap og kompetanse om kliniske studier
7. Ruste Norge for fremtidens kliniske studier, spesielt innen persontilpasset medisin
8. Gi bedre bruk av helsedata i kliniske studier
9. Øke nasjonalt og internasjonalt samarbeid om kliniske studier
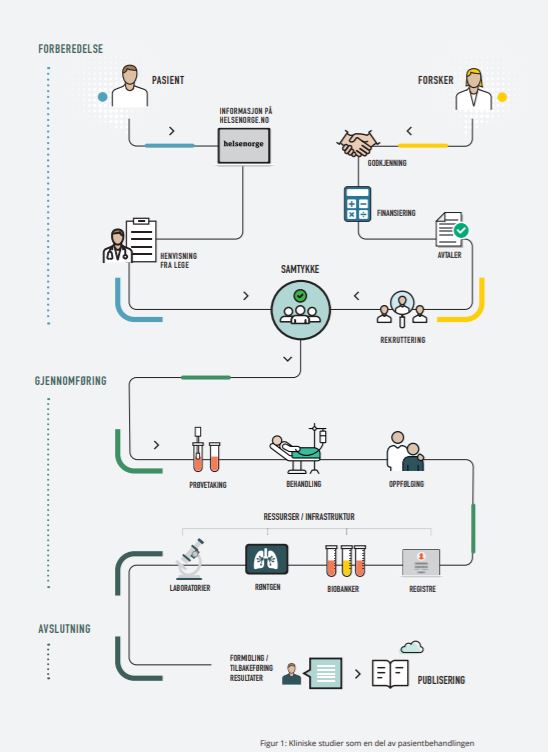
Kliniske studier gir pasientene våre tryggere og bedre behandling. Kliniske studier gir pasienter tidlig tilgang til nye legemidler og nye metoder. Kliniske studier bør derfor være en del av pasientbehandlingen.
Helseminister Bent Høie
Positive til planens visjoner
Legemiddelindustrien er godt fornøyd med planen, sa Nicolas Vaugelade Baust, leder av LMIs Forsknings- og utviklingsutvalg.
– Handlingsplanen adresserer de to hovedelementene vi i industrien mener er spesielt viktige: kultur og struktur. Det kreves et godt samarbeid mellom mange aktører for å lykkes her, og de kulturelle utfordringene det pekes på, må ikke undervurderes, så det er veldig fint at settes på kartet. Når det gjelder struktur, er vi glad for at kliniske studier skal bli en integrert del av pasientbehandlingen, sa Vaugelade Baust.
Sigbjørn Smeland, klinikkleder ved Kreftklinikken ved Oslo universitetssykehus, var også fornøyd med departementets arbeid, og understreket at de allerede i dag styrer Kreftklinikken i tråd med handlingsplanens ambisjoner og visjoner.
– Det at kliniske studier skal være en integrert del av pasientbehandlingen er sånn vi har styrt Kreftklinikken. Vi er akkreditert som Comprehensive Cancer Center, og for å bli det må 10% av pasientene være inkludert i kliniske studier. Vår ambisjon er 20%, sa Smeland.
Bør følge budsjettmidler med
Han pekte samtidig på behovet for at det følger budsjettmidler eller krav om omprioriteringer med handlingsplanen. Det samme gjorde Bjørn Tore Gjertsen, forskningsdirektør ved Haukeland universitetssjukehus i Helse Bergen. Gjertsen hadde også en rekke konkrete eksempler på flaskehalser og forbedringsområder i sitt innlegg: satelittsenter, logistikkhjelp, logiske takster, bemanning, det å bli spurt – og evnen til å svare når man blir spurt.
– Det er klart at når vi blir spurt av noen om å delta, spesielt i industristudier, så klarer vi i noen tilfeller ikke å levere et svar. Også «nei» er et svar, men vi klarer ikke engang å få dét fram tidsnok. Så det er vi nødt til å jobbe med. Det mange jeg har snakket med løfter opp, både på små og store sykehus er bemanning. Hvis man skal klare å få økt antall pasienter i kliniske studier, så må bemanningen tilpasses dette. Hvis man har en studiefinansiering så skulle det i utgangspunktet kunne løses, men mange studier finansieres etterskuddsvis, kanskje et år etter at tjenesten er levert, og det er en forretningsmodell som akademiske universitetssykehus ikke er rigget for. Så hvem er villige til å ta den investeringen?, spurte Gjertsen.
Han mener det er tre elementer som må være på plass for å lykkes: kunnskap, entusiasme og arbeidslyst.
Ambivalent positiv
Kreftforeningen er også positive til handlingsplanen, men slett ikke udelt. Generalsekretær Ingrid Stenstadvold Ross er litt ambivalent i sin dom – hun er ikke sikker på hva hun skal mene.
– Vi er veldig glade for handlingsplanen, og arbeidet departementet har gjort er utrolig viktig. For noen kreftpasienter er kliniske studier den beste muligheten for behandling som de kan få, og for noen kanskje den eneste muligheten de har igjen. Vi mener handlingsplanen leverer på mye, men den har samtidig noen mangler. Vi er alle enige om utfordringsbildet, men det er noe jeg leser i planen som jeg er usikker på om er bra eller dårlig. Det gjelder særlig de to hovedmålene. Er de ambisiøse, eller er de tamme? At andelen pasienter som deltar i kliniske studier skal være 5% i 2025 er vanskelig å vite om er ambisiøst eller tamt når vi ikke vet hva status er i dag. På enkelte områder, som på kreftområdet, kan nok dette bli tamt. Kreftsenteret ved OUS ligger jo godt over 10% i dag. Kanskje hadde det vært en ide å differensiere bildet noe. I mitt hode er det også lenge til 2025, så vi bør kanskje vurdere om vi er ambisiøse nok, eller åpne opp for å justere målet underveis. Det andre målet, om at antall kliniske studier skal dobles i perioden 2021-2025 er jeg også usikker på hva jeg skal tenke om. En dobling tar oss tilbake til det nivået vi lå på i 2000, og det oppleves ikke så ambisiøst. Samtidig handler det om å være realistisk. Kanskje er dette et greit mål likevel, sa Ross.
Ifølge Ross hadde Kreftforeningen forventet mer på en del områder. Det ene handler om viljen til å bruke ressurser på å nå målene vi alle er så enige om, det andre er bedre rådgivning og raskere godkjenning.
– Det burde vært lagt opp til en helhetlig gjennomgang av alle regelverk og prosesser som gjelder for kliniske studier. Jeg trodde egentlig vi alle var enige om det, så jeg skjønner ikke helt hvorfor det ikke står mer uttalt i planen. Og så tenker jeg at en kulturendring trenger ikke være forbeholdt sykehusene. Vi trenger en kulturendring i Statens legemiddelverk også. De bør måles på i hvilken grad de bidrar til flere kliniske studier. Det bør kanskje REK også gjøre. Og det er jo ikke for sent å få dette inn i oppdragsdokumentene til SLV for eksempel, sa generalsekretæren.
Bra at medisinsk utstyr er inkludert
Henriette Ellefsen Jovik er leder i Melanor, bransjeorganisasjonen for bedrifter som leverer medisinsk utstyr, laboratorieutstyr, måleutstyr og hjelpemidler i det norske markedet. Hun er glad for at handlingsplanen ikke utelukkende fokuserer på legemidler.
– Kliniske studier og legemidler hører tett sammen, men i Melanor er vi også glad for at handlingsplanen ikke utelukkende fokuserer på legemiddelstudier, men også spesifikt uttaler en ambisjon om at mer utprøving og forskning på utstyrsfeltet også skal skje i Norge. Noen særtrekk ved klinisk dokumentasjon og utprøving av medisinsk utstyr er blant annet at området er ekstremt bredt og variert, med om lag 500 000 ulike typer medisinsk utstyr. Det er alt utstyr som er ment for å diagnostisere, forebygge, overvåke, behandle eller lindre skade, sykdom eller funksjonsnedsettelse hos mennesker. Livssyklusen for medisinsk utstyr er kort, og preges av en konstant strøm av innovasjoner, og i 2019 var det omtrent dobbelt så mange patentsøknader på medisinsk utstyr i Europa som på legemidler. Og den vanligste livssyklusen for medisinsk utstyr er bare to år, sa Jovik.
Mange spørsmål
Det var stort engasjement og mange spørsmål under møtet. Blant annet ble Sigbjørn Smeland spurt hvordan de som sykehusledere skal få til handlingsplanens visjon om en kulturendring i sykehusene.
– Jeg mener faktisk at vi i stor grad er på vei. Men vi har jo også et godt stykke igjen. Vi skal være ambisiøse for å nå målene, og vi skal presse på slik at alt ligger til rette for at vi klarer å styrke kliniske studier.
Marianne van der Wel fra HOD ble spurt om hun kunne utdype det handlingsplanen har uttalt i forhold til ressurser til å drive studier – blant annet håndtering av inntekter fra oppdragsstudier og hvordan dette i større grad kan komme forskningsmiljøene til gode.
– Det handler egentlig om en oppklaring av hvordan man har håndtert disse inntektene tidligere, der har det vært litt ulik praksis. Blant annet har man tidligere overført disse midlene til fond eller stiftelser og avsatt midlene over flere år, for deretter å bruke dem til å finansiere egen forskning. Men det var en praksis som viste seg å være i strid med avsetningsreglene i regnskapsloven, så slike ordninger ble derfor avviklet. Så det vi sier nå er at disse midlene ikke skal overføres til fond eller stiftelser, men de kan fortsatt brukes til forskningsaktivitet ved avdelingene som har utført studien. Da må de inntektsføres fortløpende. Så dette er i praksis en avklaring, sa van der Wel.
(fra 04.45 da teknikken ikke lengre sviktet oss):
Marianne van der Wels slides fra møtet kan lastes ned her