Nå skal heldigvis deler av prosessen – «Nye metoder» – evalueres, men vi må fortsatt vente i over ett år før evalueringen er klar.
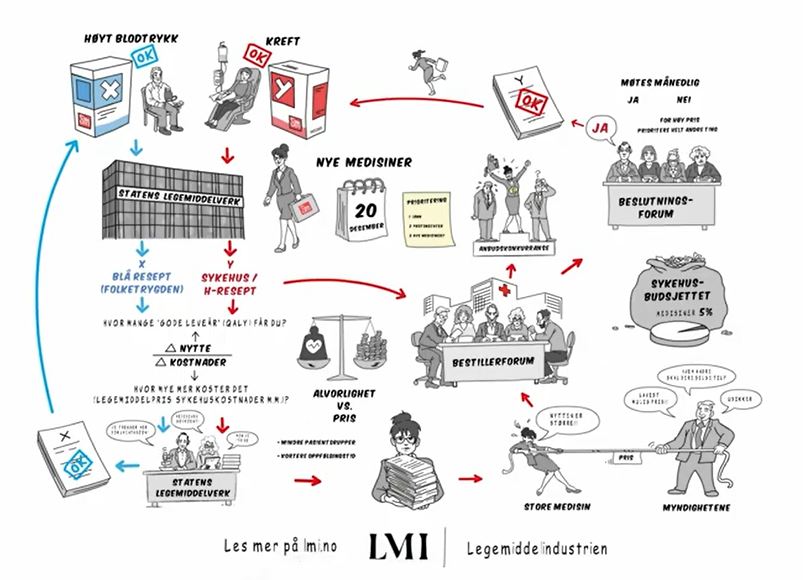
Legemiddelindustrien (LMI) har laget en skriblefilm som forklarer hvorfor det tar mange måneder og kanskje år fra en medisin får markedsføringstillatelse i Norge til den kan tas i bruk av norske pasienter. På fem minutter forklarer vi deg hele den kompliserte prosessen, med fine tegninger av illustratør Per Trystad.
(Saken fortsetter under filmen)
Men siden systemet er såpass komplisert, og det er så mange ekstra «hvis»- og «dersom»-elementer, kan du lese en mer utdypende forklaring i denne saken.
Så hva er utfordringen?
Det tar altfor lang tid. Kravet om lavest mulig pris dominerer, fagpersoner blir ikke alltid lyttet til, og systemet tar ikke hensyn til at mange nye medisiner er persontilpasset.
Hvorfor tar godkjenningsprosessen så lang tid? Det er fordi norske myndigheter først må finne ut om de vil prioritere å bruke penger på medisinen.
To ulike løp
Medisiner kan du enten betale selv på en vanlig, hvit resept, og da kan de brukes rett etter godkjennelsen fra legemiddelmyndighetene. Myndighetene kan i andre tilfeller betale hele eller deler av behandlingen. Dette gjelder medisiner som brukes over tid – enten medisiner på blå resept, som fastlegen forskriver og som dekkes av Folketrygden, eller medisin betalt av sykehusene som kun spesialister kan gi deg. I disse tilfellene ønsker myndighetene å vurdere om nytten av medisinene står i rimelig forhold til kostnadene før medisinen kan tas i bruk. Dersom sykdommen er alvorlig, er myndighetene villige til å betale mer enn om sykdommen er mindre alvorlig.
Legemiddelverket får tidlig informasjon om hvilke medisiner som er på vei til å bli medisinsk godkjent, mens Helsedirektoratet kartlegger om dette er en medisin som kan betales via blå resept eller sykehusene/h-resept. Legemiddelverket oppsummerer relevant informasjon i et notat – et metodevarsel – for hver ny medisin.
For medisiner på blå resept, er det Legemiddelverket som både vurderer nytte og kostnader, samt – i de aller fleste tilfellene – tar beslutningen om medisinen skal dekkes av myndighetene. Ved en positiv avgjørelse, kan medisinen tas i bruk kort tid etter. Unntaket er dersom Legemiddelverkets godkjenning av medisinen medfører store kostnader, over den såkalte fullmaktsgrensen på 100 millioner kroner årlig fem år etter at medisinen er tatt i bruk. Da er det Stortinget som tar den endelige avgjørelsen, og prosessen tar vesentlig lengre tid.
For medisin betalt av sykehusene, starter prosessen tidligere og er mer omfattende enn for prosessen på blå resept. Notatet fra Legemiddelverket diskuteres i Bestillerforum som er tilknyttet sykehusene, og her bestemmes veien videre for medisinen.
Bestillerforum
Bestillerforum består av de fire fagdirektørene i de regionale helseforetakene, samt to representanter fra Helsedirektoratet.
Bestillerforum har månedlige møter. Det er mulighet for både pasientorganisasjoner, produsenter og andre å gi innspill til Bestillerforum i forkant av møtet.
For medisiner som er bedre og dyrere enn de medisinene som allerede er tilgjengelig, vil Bestillerforum ofte bestemme at det skal gjøres en grundig vurdering av nytten opp mot kostnadene, selv om det i enkelte tilfeller kan «bestilles» en enklere vurdering. Ligner medisinen på en annen medisin som allerede er tilgjengelig, kan det bli bestemt at medisinen er «lik nok» til å inngå i en ren priskonkurranse – et anbud. Det er ikke alltid enighet mellom myndighetene, industrien og klinikerne om medisinen er lik nok eller ei.
Legemiddelverket
Etter møtet i Bestillerforum, skal produsenten – altså legemiddelselskapet – levere det som er bestilt av dokumentasjon, til Legemiddelverket. Noen ganger kreves mer dokumentasjon enn det som er mulig å fremskaffe, blant annet fordi den medisinske utviklingen har gått så fort at pasientgruppene nå er mindre enn før og oppfølgingstiden er kortere. Legemiddelmyndighetene godtar denne type dokumentasjon for å få medisinen medisinsk godkjent, men det er ofte ikke nok for at myndighetene sier ja til å bruke penger på medisinen. Dokumentasjonen er uansett tidkrevende for legemiddelselskapet å lage, og tidkrevende for Legemiddelverket å gå gjennom.
Dermed vokser også sakskøen hos Legemiddelverket. Her kan det også oppstå uenighet mellom Legemiddelverket og produsenten om dokumentasjonen og nytten av medisinen. Dette er spesielt aktuelt ved små sykdomsområder og/eller ved persontilpasset medisin, hvor det er færre pasienter med i kliniske studier enn det vi tidligere har vært vant til.
Maksimalpris
Når produsenten får medisinsk godkjenning for medisinen, vil de søke Legemiddelverket om en såkalt maksimalpris på medisinen. Av en gruppe på ni europeiske land, er det bestemt av norske myndigheter at denne maksimalprisen er gjennomsnittsprisen av de tre landene med lavest pris – blant landene Sverige, Finland, Danmark, Tyskland, Storbritannia, Nederland, Østerrike, Belgia og Irland.
Produsenten er etter hvert i dialog med sykehusenes innkjøpsorgan, Sykehusinnkjøp. Sykehusinnkjøp forhandler med produsentene om rabattert pris på vegne av sykehusene. Når Legemiddelverket har ferdigstilt sin evaluering, vil pristilbudet og Legemiddelverkets vurdering legges frem for sykehusene via Bestillerforum, som klargjør for avgjørelse i Beslutningsforum. Dette kan ta tid, og enkelte prinsipielle saker må også diskuteres i Bestillerforums møte før klargjørelse.
Beslutningsforum
Den endelige avgjørelsen om medisinen kan tas i bruk av norske pasienter, tas av Beslutningsforum, som består av de fire direktørene i de fire regionale helseforetakene.
Også Beslutningsforum møtes bare én gang i måneden, så om det er mange saker som skal diskuteres, kan det hende de må vente med noen avgjørelser til et senere møte. Da går tiden.
Dersom prisen vurderes som for høy i forhold til nytten, kan Beslutningsforum si nei. De kan også velge å ikke ta i bruk medisinen dersom totalkostnaden blir for høy for sykehusene, og fordi de vil prioritere å bruke penger på noe annet. Sykehusbudsjettet skal dekke alt fra dopapir og medisiner, til sykehusbygg og ansattes lønn. Men under 5 % av sykehusbudsjettet går til medisiner.
Anbudsprosess
Dersom Beslutningsforum sier ja, vil medisinen kunne tas i bruk ganske raskt etterpå, med mindre lignende medisiner allerede er i bruk på sykehusene – da må den nye medisinen delta i en anbudskonkurranse før den tas i bruk. Myndighetene arrangerer anbudskonkurranser for hvert terapiområde kun én gang i året eller sjeldnere, så dersom det nylig har blitt gjennomført en anbudskonkurranse, kan det ta opptil 1-2 år før den nye medisinen blir tilgjengelig.
Hele denne prosessen kan ta måneder og til og med år. I noen deler av prosessen er leger og annet helsepersonell – i større eller mindre grad – involvert. Noen ganger blir de hørt, andre ganger ikke.
Bærekraftig helsetjeneste
Vi er alle tjent med en bærekraftig helsetjeneste, og nye medisiner kan bidra til nettopp det. Samfunnsutviklingen tilsier at det framover må satses mer på nye legemidler og annen helseteknologi. Kortsiktige besparelser ved ikke å ta i bruk ny teknologi, kan bli dyrt for en helsetjeneste som må omstilles. Også helseminister Bent Høie er klar på at vi trenger å samarbeide om å utvikle ny teknologi for å få en bærekraftig helsetjeneste i fremtiden. Men det hjelper lite å utvikle ny teknologi dersom vi ikke tar den i bruk. Er det riktig at alt fokuset på prioritering legges på legemidler, som altså bare utgjør 5 % av sykehusbudsjettet?
Systemet skal evalueres
Vi i legemiddelindustrien er glad for at Nye metoder – som inkluderer Bestillerforum og Beslutningsforum – nå skal evalueres, slik at det kan videreutvikles. Det er Stortinget som har bestemt dette, for å sikre alle pasienter likeverdig, trygg og effektiv tilgang på nye metoder.
– Det er viktig for meg at pasienter, fagmiljøer og leverandører blir hørt. Erfaringene og kompetansen de sitter med er viktig å lytte til når vi skal ruste Nye metoder for framtiden, sier Bent Høie.
Evalueringen skal leveres innen 31. oktober 2021, så vi må smøre oss med tålmodighet og håpe at noen grep tas før den tid også.
Noen pasienter har god tid. Andre har det ikke.